藥物涂層球囊擴(kuò)張導(dǎo)管在我國按照藥械組合產(chǎn)品注冊管理����,注冊流程與第三類醫(yī)療器械注冊流程相同。本文從注冊注冊質(zhì)量管理體系建設(shè)和核查角度����,為大家介紹藥物涂層球囊擴(kuò)張導(dǎo)管注冊質(zhì)量管理體系核查要點(diǎn),一起看正文����。
藥物涂層球囊擴(kuò)張導(dǎo)管在我國按照藥械組合產(chǎn)品注冊管理,注冊流程與第三類醫(yī)療器械注冊流程相同����。本文從注冊注冊質(zhì)量管理體系建設(shè)和核查角度,為大家介紹藥物涂層球囊擴(kuò)張導(dǎo)管注冊質(zhì)量管理體系核查要點(diǎn)����,一起看正文。
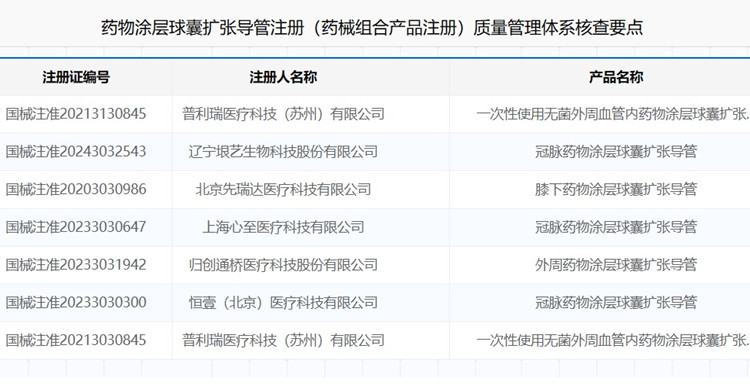
藥物涂層球囊擴(kuò)張導(dǎo)管注冊質(zhì)量管理體系核查要點(diǎn)
一����、藥物涂層球囊擴(kuò)張導(dǎo)管作用機(jī)理
藥物涂層球囊擴(kuò)張導(dǎo)管預(yù)防和治療血管再狹窄的機(jī)理����,主要為在球囊擴(kuò)張時(shí)將藥物直接輸送到病變血管壁����,實(shí)現(xiàn)局部藥物治療。通過球囊的物理擴(kuò)張作用����,藥物能夠以高濃度
直接作用于病變部位,減少了全身性藥物副作用的風(fēng)險(xiǎn)����。根據(jù)使用部位的不同,可分為藥物涂層冠脈球囊擴(kuò)張導(dǎo)管����、藥
物涂層外周球囊擴(kuò)張導(dǎo)管等。根據(jù)藥物種類的不同����,主要可分為紫杉醇類藥物、雷帕霉素類藥物����、其他藥物等類型����。
二����、藥物涂層球囊擴(kuò)張導(dǎo)管結(jié)構(gòu)組成
不同企業(yè)的產(chǎn)品結(jié)構(gòu)組成各有不同����,但一般由球囊擴(kuò)張
導(dǎo)管主體和藥物涂層組成。球囊平直段涂覆藥物涂層����。產(chǎn)品結(jié)構(gòu)示意圖(以 Rx 型為例)見圖 1。

2.1球囊擴(kuò)張導(dǎo)管
根據(jù)球囊導(dǎo)管交換的類型����,分為整體交換型(OTW 型)
球囊擴(kuò)張導(dǎo)管與快速交換型(Rx 型)球囊擴(kuò)張導(dǎo)管。一般由
尖端����、球囊、顯影標(biāo)記����、內(nèi)腔管����、遠(yuǎn)端管����、過渡管、海波管����、
應(yīng)力支撐管、手柄(或“座”)和親水涂層(如適用)組成����。
2.2 藥物涂層
包括藥物、載藥基質(zhì)和/或輔料����。
常見的藥物包括紫杉
醇、雷帕霉素等����。載藥基質(zhì)是指任何不涉及活性細(xì)胞的有機(jī)
或無機(jī)材料,預(yù)期用于藥物涂層球囊擴(kuò)張導(dǎo)管并設(shè)計(jì)用于藥
物儲(chǔ)存����,器械表面局部形成藥物活性和/或促進(jìn)����、阻止����、延
遲或修改藥物釋放特性的目的����。輔料是指除藥物活性成分之
外額外添加的物質(zhì),為藥物涂層球囊擴(kuò)張導(dǎo)管產(chǎn)品含藥部分
的預(yù)期添加的成分����,如填充劑、增亮劑����、稀釋劑、潤濕劑����、
溶劑、著色劑����、穩(wěn)定劑����、抗氧化劑����、防腐劑、pH 保持劑����、聚
合物、粘著劑等����。
三、預(yù)期用途(示例)
以一款已上市的藥物涂層冠脈球囊擴(kuò)張導(dǎo)管為例:適用
于原發(fā)冠狀動(dòng)脈分叉病變狹窄的擴(kuò)張治療����。
以一款已上市的藥物涂層外周球囊擴(kuò)張導(dǎo)管為例:適用
于對患有股淺動(dòng)脈(SFA)和胸動(dòng)脈(PPA)狹窄或閉塞病變
的患者進(jìn)行經(jīng)皮腔內(nèi)血管成形術(shù)。
四����、規(guī)格型號(hào)
不同企業(yè)生產(chǎn)的產(chǎn)品對規(guī)格型號(hào)的劃分各有不同。規(guī)格
型號(hào)一般通過導(dǎo)管長度����、球囊直徑����、球囊長度等進(jìn)行劃分����。
五、產(chǎn)品性能(參考技術(shù)指標(biāo))
5.1 球囊導(dǎo)管性能
5.1.1 外觀
5.1.2 尺寸
5.1.3 末端頭端
5.1.4 柔順性
5.1.5 推送性
5.1.6 導(dǎo)絲兼容性
5.1.7 導(dǎo)引導(dǎo)管兼容性
5.1.8 耐腐蝕性
5.1.9 手柄(座)
5.1.10 無泄漏
5.1.11 峰值拉力
5.1.12 球囊充壓時(shí)間
5.1.13 球囊卸壓時(shí)間
5.1.14 球囊額定爆破壓
5.1.15 球囊額定疲勞
5.1.16 球囊直徑與充盈壓力關(guān)系
5.1.17 側(cè)孔數(shù)量及位置(如適用)
5.2 藥物涂層性能
5.2.1 藥物定性鑒別
5.2.2 載藥量/劑量密度
5.2.3 藥物體外釋放率
5.2.4 溶劑殘留
5.2.5 不溶性微粒
5.3 與產(chǎn)品配套提供的附件性能(如有)
5.4 化學(xué)性能
(產(chǎn)品技術(shù)要求應(yīng)標(biāo)注化學(xué)性能酸堿度����、蒸發(fā)殘?jiān)?���、還原物
質(zhì)、紫外吸光度是否為含藥物涂層/親水涂層(如適用)的
產(chǎn)品)
5.4.1 酸堿度
5.4.2 重金屬
5.4.3 蒸發(fā)殘?jiān)?nbsp;
5.4.4 還原物質(zhì)
5.4.5 紫外吸光度
5.4.6 環(huán)氧乙烷殘留量(如適用)
5.5 微生物性能
5.5.1 無菌
5.5.2 細(xì)菌內(nèi)毒素
六����、適用標(biāo)準(zhǔn)
GB/T 1962.1 注射器、注射針及其他醫(yī)療器械 6%(魯爾)
圓錐接頭 第 1 部分:通用要求
GB/T 1962.2 注射器����、注射針及其他醫(yī)療器械 6%(魯爾)
圓錐接頭 第 2 部分:鎖定接頭
GB 8368 一次性使用輸液器 重力輸液式
GB/T 14233.1 醫(yī)用輸液、輸血����、注射器具檢驗(yàn)方法 第
1 部分:化學(xué)分析方法
GB/T 14233.2 醫(yī)用輸液����、輸血����、注射器具檢驗(yàn)方法 第
2 部分:生物學(xué)試驗(yàn)方法
GB/T 14233.3 醫(yī)用輸液、輸血����、注射器具檢驗(yàn)方法 第
3 部分:微生物學(xué)試驗(yàn)方法
GB/T 16886 醫(yī)療器械生物學(xué)評(píng)價(jià) 系列標(biāo)準(zhǔn)
GB 18279.1 醫(yī)療保健產(chǎn)品滅菌 環(huán)氧乙烷 第 1 部分:醫(yī)
療器械滅菌過程的開發(fā)、確認(rèn)和常規(guī)控制的要求
GB/T 18279.2 醫(yī)療保健產(chǎn)品滅菌 環(huán)氧乙烷 第 2 部分:
GB 18279.1 應(yīng)用指南
GB 18280.1 醫(yī)療保健產(chǎn)品滅菌 輻射 第 1 部分:醫(yī)療器
械滅菌過程的開發(fā)����、確認(rèn)和常規(guī)控制要求
GB 18280.2 醫(yī)療保健產(chǎn)品滅菌 輻射 第 2 部分:建立滅
菌劑量
GB/T 18280.3 醫(yī)療保健產(chǎn)品滅菌 輻射 第 3 部分:劑量
測量指南
GB/T 19633.1 最終滅菌醫(yī)療器械包裝 第 1 部分:材料、
無菌屏障系統(tǒng)和包裝系統(tǒng)的要求
GB/T 19633.2 最終滅菌醫(yī)療器械包裝 第 2 部分:成形����、
密封和裝配過程的確認(rèn)的要求
GB/T 19973.1 醫(yī)療器械的滅菌微生物學(xué)方法 第 1 部分:
產(chǎn)品上微生物總數(shù)的測定
GB/T 19973.2 醫(yī)療器械的滅菌 微生物學(xué)方法 第 2 部
分:用于滅菌過程的定義、確認(rèn)和維護(hù)的無菌試驗(yàn)
GB/T 19335 一次性使用血路產(chǎn)品 通用技術(shù)條件
GB/T 23694 風(fēng)險(xiǎn)管理 術(shù)語
GB/T 39381.1 心血管植入物 血管藥械組合產(chǎn)品 第 1 部
分:通用要求
GB/T 42061 醫(yī)療器械 質(zhì)量管理體系 用于法規(guī)的要求
GB/T 42062 醫(yī)療器械 風(fēng)險(xiǎn)管理對醫(yī)療器械的應(yīng)用
YY/T 0033 無菌醫(yī)療器具生產(chǎn)管理規(guī)范
YY 0285.1 血管內(nèi)導(dǎo)管一次性使用無菌導(dǎo)管 第 1 部分:
通用要求
YY 0285.4 血管內(nèi)導(dǎo)管一次性使用無菌導(dǎo)管 第 4 部分:
球囊擴(kuò)張導(dǎo)管
YY 0450.1 一次性使用無菌血管內(nèi)導(dǎo)管輔件 第 1 部分:
導(dǎo)引器械
YY/T 0586 醫(yī)用高分子制品 X 射線不透性試驗(yàn)方法
YY/T 0663.2 心血管植入物 血管內(nèi)器械 第 2 部分:血
管支架
YY∕T 0916.7 醫(yī)用液體和氣體用小孔徑連接件 第 7 部
分:血管內(nèi)或皮下應(yīng)用連接件
YY/T 1437 醫(yī)療器械
GB/T 42062 應(yīng)用指南
YY/T 1737 醫(yī)療器械生物負(fù)載控制水平的分析方法
中國藥典
如有藥物涂層球囊擴(kuò)張導(dǎo)管注冊����、藥物涂層球囊擴(kuò)張導(dǎo)管產(chǎn)品技術(shù)要求、藥械組合產(chǎn)品注冊����、醫(yī)療器械注冊����、醫(yī)療器械質(zhì)量管理體系咨詢服務(wù)需求����,歡迎您隨時(shí)方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò),聯(lián)系人:呂工����,電話:18058734169,微信同����。